Terapia moleculară țintită permite distrugerea celulelor canceroase, cu mai puține reacții adverse, eficiență crescută, îmbunătățirea calității vieții. În cadrul Spitalului Clinic Județean de Urgență (SCJU) Târgu Mureș, printr-un proiect de cercetare, pacienții cu cancer gastrointestinal, operați în cadrul spitalului, beneficiază de determinări de biologie moleculară pentru identificarea terapiei țintite în funcție de gena mutantă. Analizele sunt gratuite pentru patru ani de zile, însă s-au făcut demersuri la nivelul Ministerului Sănătății și a Casei Naționale de Asigurări de Sănătate (CNAS) pentru a fi realizat ”un program național de oncologie prin care să se poată face gratuit aceste determinări în centrele în care există dotări”. Despre proiectul de cercetare, dotările existente în cadrul SCJU Târgu Mureș și direcțiilor de dezvoltare în viitorul apropiat a oferit mai multe detalii Prof. Dr. Simona Gurzu, șeful Serviciului de Anatomie Patologică din cadrul SCJU Târgu Mureș.
Reporter: La nivelul SCJU Târgu Mureș se fac analize gratuite de biologie moleculară pentru cancerul gastrointestinal, în cadrul unui proiect de cercetare. Vă rog să oferiți mai multe detalii despre acest proiect.
Prof. Dr. Simona Gurzu: Proiectul Complex de Cercetare de Frontieră GRAPHSENSGASTROINTES se realizează în colaborare cu Prof. Dr. Raluca-Ioana van Staden de la Institutul Național de Cercetare Dezvoltare pentru Electrochimie și Materie Condensată din București și Prof. Dr. Stela Maria Pruneanu de la Institutul Național de Cercetare Dezvoltare pentru Tehnologii Izotopice și Moleculare din Cluj Napoca. Este un proiect ambițios, care ia în calcul determinarea biomarkerilor moleculari la pacienții cu cancer gastrointestinal. Scopul principal este găsirea unor noi metode de identificare a acestor biomarkeri din salivă, urină și sânge folosind senzori stocastici, care sunt sintetizați de către coordonatorul de proiect de la București.
Povestea proiectului a început în anul 2012, când am câștigat o bursă de cercetare L’Oreal, în juriu fiind chiar Prof. Dr. van Staden, coordonatorul proiectului. Atunci am înființat practic un laborator de Oncopatologie Moleculară (n.red. – în cadrul SCJU Târgu Mureș) care a devenit funcțional în anul 2017, în momentul în care în echipă a fost inclus și geneticianul, Dr. Kovacs Zsolt, pentru că fără un genetician nu poți să pornești un astfel de proiect. Proiectul a fost câștigat în anul 2018.
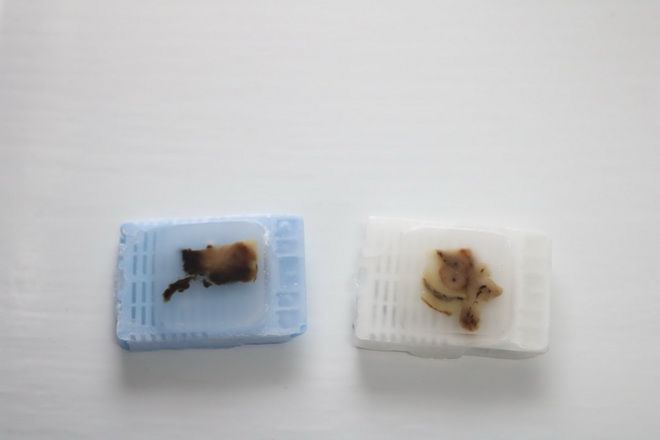
Ce facem noi în cadrul acestui proiect? În primul rând, în laborator există dotarea de bază. În 2012, aveam un PCR și accesoriile pentru izolarea și cuantificarea ADN-ului. Cu sprijin din partea spitalului, s-a cumpărat încă un PCR și un congelator de păstrare a țesuturilor la -80°C, pentru că țesuturile, pentru a fi prelucrate molecular, este bine să fie proaspete, păstrate la -80°C. Din noiembrie 2018 am început să determinăm markerii moleculari în scop diagnostic și terapeutic.
Scopul final al proiectului este sinteza senzorilor stocastici. Ideea este să reușești să determini acești biomarkeri moleculari cu un preț cât mai mic. Dar până atunci, firesc este să compari rezultatele pe senzori stocastici cu metodele care există deja pe piață. Și ne-am gândit cum am putea ajuta pacientul. Am stabilit împreună cu managerul spitalului, cu rectorul UMFST ”George Emil Palade” și șefii de la secțiile de chirurgie o colaborare, cu acordul Comisiei de etică. Astfel, de la pacienții cu cancer gastric și colorectal, la care chirurgii ne trimit piesa proaspătă, putem să facem gratuit, fără niciun cost din partea pacientului, determinări de biologie moleculară.
Rep: De ce sunt importante aceste determinări de biologie moleculară?
S.G.: Trăim într-o perioadă în care vorbim de terapie individualizată, asta înseamnă că în funcție de ce genă este mutantă la un pacient cu cancer, pacientul poate beneficia de tratament personalizat, individualizat.
În prezent, am efectuat aceste determinări la peste 70 de cazuri și mai am avem vreo 10 în laborator, deci trecem de 80 de cazuri de pacienți cu cancer gastric și colorectal care au primit un buletin histopatologic complex, în care am inclus diagnosticul histopatologic dar și toată informația moleculară de care au nevoie pentru terapia personalizată. Din luna septembrie 2019 am stabilit în cadrul proiectului o colaborare cu o firmă privată prin care pacientului i se determină, din sânge, gratuit patru markeri moleculari cu rol prognostic și predictiv.
Așadar, la același pacient, determinăm biomarkerii din sânge și țesut și în același timp se trimit probe biologice la București și prin metode chimice/biochimice se încearcă sintetizarea unor senzori care să scadă costurile de determinare a acestor biomarkeri.
Se încearcă sintetizarea unui aparat care poate să identifice non-invaziv și cu costuri minime ceea ce noi determinăm prin tehnici moleculare scumpe.
Rep.: Pe ce perioadă se asigură gratuit determinările de biologie moleculară?
S.G.: Proiectul asigură finanțare pentru aceste determinări pentru patru ani de zile, respectiv 2019-2022. Firesc, ne-am gândit ce se va întâmpla ulterior. Cu acordul managerului SCJU Târgu Mureș, am început demersurile la Ministerul Sănătății pentru includerea acestor servicii în contractul cu CNAS. În prezent, determinările de biologie moleculară nu doar că sunt suportate de căre pacient sau uneori de către firme de medicamente, dar procesul este prelungit deoarece se dă diagnosticul histopatologic în laborator, după care pacientul trebuie să vină să își ia blocul de parafină, care include țesuturi, se duce la un alt laborator în care se fac determinări de biologie moleculară și timpul se prelungește foarte mult până ce el are un diagnostic complet și poate să înceapă terapia. Vorbim despre un pacient cu cancer în stadiu avansat la care fiecare zi de întârziere a instituirii terapiei înseamnă șanse mai mici de răspus dar și costuri mai mari din partea spitalelor.
Sunt și situații în care pacientul nu mai vine să-și ia țesutul, nu mai face determinările de biologie moleculară și nu beneficiază de acest tratament, deși el există în spitalele de oncologie.
Am încercat să convingem reprezentanții Ministerului Sănătății să introducă în contractul cu CNAS aceste determinări. Am reușit să trecem propunerea de Comisiile Naționale de Anatomie patologică și Oncologie și în prezent documentația este la CNAS. Noi am propus un program național de oncologie prin care să se poată face determinări gratuite în centrele în care există dotări. Acum s-a schimbat conducerea la CNAS și va trebui să reîncepem demersurile. Sperăm ca propunerea noastră să fie acceptată, să obținem susținere și de la Asociația Bolnavilor de Cancer din România și pacientul oncologic să beneficieze de toate determinările de care beneficiază și în afara țării. Terapia este gratuită, dar în acest moment determinările necesare acestei terapii nu sunt susținute de CNAS.
Rep.: Acest tratament personalizat acordat în urma determinărilor de biologie moleculară, în ce cazuri este recomandat?
S.G.: Tratamentul personalizat se administrează mai ales pacienților cu metastaze sau recidive. În cazul cancerului de colon tratamentul constă fie în perfuzii cu citostatice, fie în medicamente administrate per oral. La pacientul cu cancer, medicamentele țintite molecular asigură o calitate a vieții foarte bună și supraviețuirea crește semnificativ.
Rep.: Prin aceste determinări puteți identifica exact ce fel de tratament trebuie să urmeze.
S.G.: Așa este. Spre exemplu, în cancerul de colon determinările moleculare vizează două gene: gena KRAS și BRAF. Pacienții care nu prezintă mutații ale genei KRAS, și majoritatea dintre ei nu prezintă mutații, pot primi tratamentul cu așa numitul Cetuximab sau derivați care inhibă gena EGFR. Dacă prezintă mutații atunci nu pot primi tratamentul pentru că nu îmbunătățește calitatea vieții și pacienții nu răspund la tratament. Mai există gena BRAF, care este mutantă de obicei la pacienții care prezintă așa numita instabilitate microsatelitară (MSI). Am reușit la nivel de spital să convingem conducerea să asigure fondurile pentru determinarea statusului MSI prin metode imunohistochimice. Dacă pacientul prezintă instabilitate microsatelitară s-ar putea ca gena BRAF să fie mutantă și nu poate primi tratamentul cu 5 Fluorouracil, tratament care se administrează de obicei la acești pacienți. Dacă prezintă mutații ale genei BRAF primește medicamente anti-BRAF. Practic este un algoritm de diagnostic și tratament, iar prin aceste determinări de biologie moleculară poți să ajuți la terapia individualizată, care se practică în toate spitalele de oncologie din țară. Oriunde se duce cu un astfel de diagnostic poate primi terapia individualizată, în România tratamentul fiind suportat de către CNAS.
Noi, în dotarea laboratorului avem tot ce ne trebuie pentru aceste determinări de biologie moleculară. Urmează să mai fie achiziționate două aparate, care sunt trecute de procesul de licitație publică și sperăm că anul viitor se vor achiziționa. Unul dintre aparate este pentru testarea calității ADN-ului. Ideal este ca atunci când faci determinări de biologie moleculară să le faci din țesut proaspăt și nu este mereu ușor deoarece operațiile se desfășoară și în weekend sau după amiaza și atunci piesele se includ în formol. Dacă s-a inclus piesa în formol eu nu mai pot să fac determinarea din țesut proaspăt și următorul pas în prepararea tehnică este să includ piesa în parafină, dar aici riscul este ca ADN-ul să fie degradat și să nu mai am șansa să identific acele mutații genetice. Avem nevoie de un aparat care să testeze calitatea ADN-ului pentru ca atunci când calitatea ADN-ului nu este bună să nu trec la pasul următor, să fac determinări, pentru că fie nu am nicio șansă să identific mutația sau pot să am rezultat fals pozitiv sau fals negativ. Astfel, evit costurile nejustificate.
Al doilea aparat este un secvențiator genic de tip Sanger. În prezent, cu aparatele pe care le avem, putem determina mutații la nivelul unei singure gene și dacă vreau să determin și KRAS și BRAF trebuie să pun de două ori proba. Secvențierea îmi permite să includ un panel de gene și pot să identific nu doar mutația ci și localizarea acesteia. În plus, am putea extinde aria determinărilor și la alte tipuri de cancer, în afara celui gastrointestinal.
Rep.: Intenționați să lărgiți panelul de gene și pe alte tipuri de cancer?
S.G.: Firesc, progresele în oncologie te obligă să identifici nu doar existența mutației, ci și exonul interesat. De exemplu, în cazul tumorilor stromale gastrointestinale (GIST) nu este suficient să știi dacă pacientul are sau nu mutație a genei c-KIT ci, mergând mai departe și văzând ce exon este mutant, se stabilește nu doar medicamentul ci și doza pe care pacientul poate să o primească, în funcție de exonul interesat.
Ambiția este să aducem în sistemul de stat examinările genetice și pe viitor, în afară de cancerele gastrointestinale, ar trebui să avem un panel pe patologia ginecologică, hematologică, neurologică, melanoame, un panel minim pe toate tumorile solide, atît din țesut proaspăt cât și din cel inclus în parafină.
Întrucât calitatea țesutului depinde de prelucrarea pre-PCR iar blocurile de parafină cu țesut se păstrează timp îndelungat în arhivă, anul acesta am achiziționat un aparat de vidat pungi care permite păstrarea țesutului în formol, în mediu ermetic, cu șanse mai mari de conservare a ADN-ului. De la 1 ianuarie 2020 vom implementa și o arhivare digitală a țesuturilor care se stochează în Arhiva Serviciului de Anatomie Patologică.
Suntem, cred, singurul spital de stat din România, care are în cadrul Serviciului de Anatomie Patologică acest sistem de arhivare. Întrucât trebuie să păstrăm blocurile de parafină pentru 30 de ani, dacă pacientul vine și cere blocul respectiv trebuie să-l punem la dispoziție. Și căutăm în arhiva în care se stochează zilnic peste 150-200 de casete histologice. Pe aceste casete se va imprima un cod de bare care va fi scanat de un sistem care favorizează formarea unei baze de date automate și apoi, cu un scaner mobil, dacă vrei să cauți un astfel de bloc în arhivă îl poți identifica după codul de bare.
Rep.: În ce situații este necesară identificarea rapidă a țesutului?
S.G.: Sunt situații în care pacientul a trăit 4-5 ani fără o recidivă a tumorii, apoi apare o metastază și trebuie să fie revăzut țesutul inițial. Și în momentul acela pacientul vine și solicită determinări suplimentare din blocul de parafină. Pentru pacient nu e totuna că i-l dai în aceeași zi sau după o săptămână sau o lună. Noi încercăm de fiecare dată să punem blocul la dispoziția pacientului în aceeași zi. Sper ca în scurt timp să creștem nivelul de performanță în oncologie și prin aceste determinări efectuate în sistemul de stat.
A consemnat Arina TOTH